Inseticidas são ferramentas essenciais na proteção de culturas agrícolas, inclusive da soja. Os ingredientes ativos disponíveis atualmente são classificados pelo Comitê de Ação contra Resistência a Inseticidas (IRAC) em cerca de 30 grupos diferentes, cada qual apresentando um modo de ação distinto. Hoje iniciaremos o estudo da terceira grande classe de modos de ação de inseticidas: produtos que atuam no processo de respiração celular dos insetos. Para isso, precisamos primeiro compreender como ocorre a metabolização de energia nas células dos insetos, e dos animais como um todo.
Certos insetos são considerados pragas porque consomem as calorias destinadas à nossa alimentação. A caloria é uma medida de energia, que os insetos obtém através dos mesmos nutrientes que nós: carboidratos, lipídios e proteínas, quebradas por enzimas do sistema digestivo em moléculas menores de açúcares, aminoácidos e ácidos graxos, respectivamente. Essas moléculas são então transportadas pela hemolinfa (o sangue dos insetos) até todas as células do corpo, que as processam em estruturas intracelulares denominadas mitocôndrias para converter em uma forma padrão de energia, passível de ser utilizada em todos os processos celulares. Essa “moeda energética” das células é a molécula de adenosina trifosfato (ATP), que armazena a energia oriunda dos nutrientes na ligação química entre os dois últimos fosfatos da sua cadeia trifosfato. Moléculas de ATP fornecem energia para outras moléculas fosforilando-as (ou seja, doando um grupo fosfato) e tornando-se ADP (adenosina difosfato); subsequentemente, a ADP é fosforilada pela mitocôndria e torna-se ATP novamente.
Todas as células animais e vegetais possuem mitocôndrias, que evoluíram a partir de bactérias simbiontes a milhares de anos. O seu tamanho em relação à célula inteira é comparável ao nosso tamanho em relação a um campo de futebol. Células musculares, que demandam uma grande quantidade de energia, podem conter milhares de mitocôndrias. Essencialmente, essas estruturas podem ser comparadas a uma usina de energia termelétrica: ambas queimam combustível para obter sua energia química em uma forma utilizável. O processo de combustão nada mais é do que a liberação de energia em uma sequência de reações químicas entre um combustível e um oxidante, que geralmente é o oxigênio. Na usina de energia, o carvão é queimado com o oxigênio para liberar calor e mover turbinas de geração de energia a vapor; na “usina celular” (mitocôndria), ocorre a combustão (queima) dos nutrientes com oxigênio para fosforilar as moléculas de ATP. Em ambos os casos, dióxido de carbono (CO2) é produzido como um resíduo. Esse processo todo é denominado respiração celular, por assemelhar-se à inalação e exalação dos pulmões que geralmente associamos à respiração. De fato, as mitocôndrias consomem a maior parte do oxigênio que inalamos, e produzem a maior parte do CO2 que exalamos.
As mitocôndrias apresentam membranas externas e internas, formando um espaço intermembrana separado da matriz mitocondrial (Figura 1). Nutrientes são oxidados (queimados) na matriz mitocondrial em um processo bioquímico denominado Ciclo de Krebs, gerando energia na forma de ATP, NADH (nicotinamida adenina dinucleotídeo) e FADH2 (flavina adenina dinucleotídeo). Já na membrana interna da mitocôndria, quatro grandes complexos protéicos, em conjunto com as moléculas de coenzima Q (CoQ) e citocromo C (CytC), formam uma cadeia de transporte de elétrons. Elétrons existem nas moléculas em níveis específicos de energia, e sua transferência entre moléculas envolve também a transferência dessa energia. Elétrons altamente carregados do NADH entram na cadeia de transporte pelo Complexo I, enquanto os elétrons oriundos do FADH2 entram via Complexo II. Após passarem pela cadeia de transporte, eles são unidos a um átomo de oxigênio para formar uma molécula de água no Complexo IV. A energia derivada desse transporte é utilizada para bombear íons através da membrana mitocondrial interna (no sentido da matriz para a intermembrana), criando um gradiente de íons com capacidade de realizar trabalho, já que os íons tendem a mover-se naturalmente de um estado ordenado (alta concentração) para um desordenado (baixa concentração). Essa tendência é denominada princípio da entropia.
Figura 1. Célula animal, mitocôndria e cadeia de transporte de elétrons na membrana mitocondrial interna.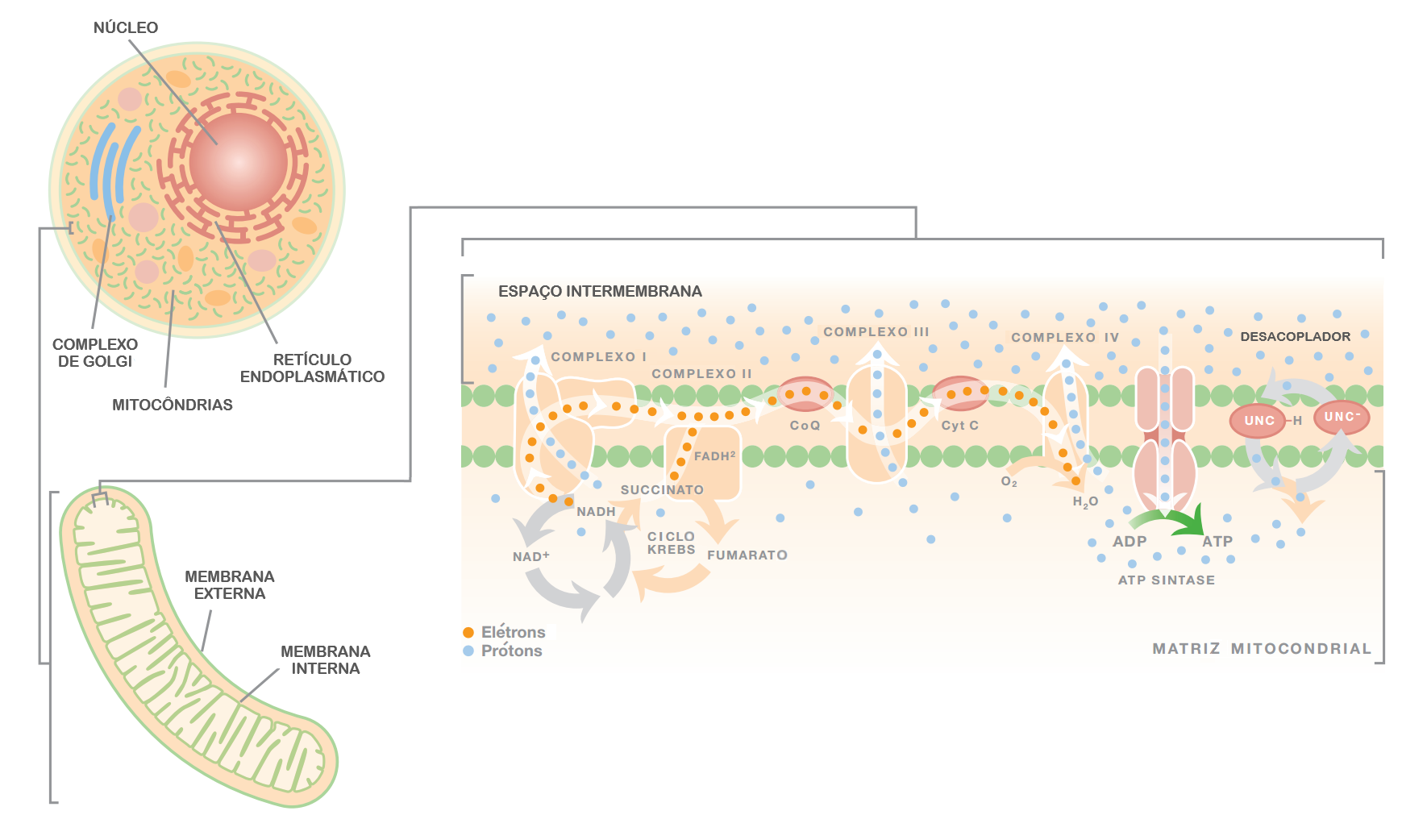
Fonte: SALGADO, V. L. (2013). Confira a imagem original clicando aqui
Os íons bombeados pelos complexos de transporte de elétrons são prótons (ou seja, os núcleos de átomos de hidrogênio), que estão sempre presentes em soluções aquosas como resultado da dissociação de moléculas de água, conferindo as características de acidez (o pH nada mais é do que uma medida da concentração de prótons). A enzima mitocondrial responsável por fosforilar as moléculas de ADP e transformá-las em ATP, utilizando a energia oriunda do gradiente de prótons, é denominada ATP-sintase (ou F0F1-ATPase). Estruturalmente, essa enzima pode ser descrita como dois motores giratórios conectados por um eixo: o fluxo de prótons do espaço intermembrana (alta concentração) para a matriz (baixa concentração) através do motor F0 gera uma força de rotação no motor F1, impulsionando a forsforilação de ADP em ATP na matriz mitocondrial. Esse processo é denomimado fosforilação oxidativa. Todos os inseticidas que afetam a respiração celular atuam na membrana mitocondrial interna, seja inibindo a ATP-sintase, interrompendo algum dos complexos de transporte de elétrons, ou desacoplando a oxidação da fosforilação ao tornar a membrana permeável aos prótons (e, portanto, incapaz de manter um gradiente de íons). Embora os seis grupos de inseticidas gerem o mesmo efeito final (interrupção da síntese de ATP e falência energética das células), eles o fazem por diferentes mecanismos, oferecendo uma ampla variedade de sítios de ação.
Inicialmente, falaremos sobre os inseticidas e acaricidas pertencentes ao Grupo 12, que inibem diretamente a enzima ATP-sintase. Diafentiuron, o ingrediente ativo mais conhecido desse grupo, é um acaricida e inseticida de amplo espectro registrado pra uso em soja, algodão, olerícolas, frutíferas e ornamentais. Controla todas as fases de vida dos ácaros, pulgões e mosca-branca. Trata-se na verdade de um pro-inseticida, que precisa ser convertido em sua forma ativa para desempenhar a ação de controle. Essa ativação pode ocorrer na superfície foliar (catalisada pela luz) ou no interior do inseto (catalisada pelas mono-oxigenases P450). A forma ativada do diafentiuron bloqueia a passagem de prótons na subunidade F0 da ATP-sintase, interrompendo seu funcionamento.
Por controlar as principais pragas sugadoras e também os ácaros, com praticamente nenhum efeito sobre insetos benéficos, diafentiuron é considerado uma ferramenta única e valiosa no manejo integrado de pragas (MIP), principalmente na cultura do algodão. Sua toxicidade é baixa para mamíferos e aves, e embora apresente efeito sobre peixes, sofre rápida degradação no ambiente. Não há casos relatados de resistência a diafentiuron desde seu lançamento em 1991.
Já os inseticidas organoestânicos (azociclotina, cihexatina e fenbutatina) diferenciam-se por conter átomos de metal na sua composição. São eficientes no controle de todas as fases de vida dos ácaros fitófagos, inclusive em populações resistentes a outros acaricidas, além de entregar longo efeito residual. Assim como o diafentiuron, esses ingredientes ativos bloqueiam a subunidade F0 da ATP-sintase. Casos de resistência já foram reportados, embora não ocorram por alteração do sítio de ação. Os inseticidas organoestânicos apresentam toxicidade baixa para aves e artrópodes benéficos, e alta para organismos aquáticos (incluindo peixes, algas e invertebrados). Em mamíferos a toxicidade aguda é baixa, mas pode ocorrer toxicidade crônica e danos à visão.
Por fim, os ingredientes ativos propargite e tetradifon controlam ovos e estágio imaturos de ácaros. Embora sejam não-sistêmicos, apresentam longo efeito residual. A inibição da ATP-sintase ocorre, também, por inativação da subunidade F0 da enzima. Ambos os produtos são considerados não-tóxicos para insetos benéficos, embora propargite apresente toxicidade sobre peixes e invertebrados aquáticos, além de irritação aos olhos em humanos. Casos de resistência por alteração do sítio de ação não são conhecidos.
Portanto, os inibidores da ATP-sintase representam importantes ferramentas no controle de pragas agrícolas, especialmente ácaros fitófagos. Seu potencial para desenvolvimento de resistência pode ser considerado baixo, principalmente no caso do diafentiuron. Para um correto posicionamento desses produtos, consulte sempre um engenheiro agrônomo. Na próxima semana, entenderemos o funcionamento do clorfenapir e outros inseticidas pertencentes ao Grupo 13: desacopladores da fosforilação oxidativa.
A reprodução desse texto, ou partes dele, deve ser precedida de autorização dos autores e acompanhada de citação da seguinte fonte: POZEBON, H.; ARNEMANN, J. A. Como funcionam os inseticidas inibidores da respiração celular? Portal Mais Soja. 2021. Disponível online.
Revisão: Prof. Jonas Arnemann, PhD. e coordenador do Grupo de Manejo e Genética de Pragas – UFSM
REFERÊNCIAS:
SALGADO, V. L. 2013. BASF Insecticide Mode of Action Technical Training Manual. Disponível em:https://agriculture.basf.com/global/assets/en/Crop%20Protection/innovation/BASF_Insecticide_MoA_Manual_2014.pdf
IRAC. 2018. Mode of Action Classification Scheme.
Disponível em: https://www.irac-online.org/documents/moa-structures-poster-english/?ext=pdf




