Autores: Marcelo Nicolai, Acácio Gonçalves Netto, Saul Jorge Pinto de Carvalho, Laís Sousa Resende, Jéssica Cursino Presoto, Jeisiane de Fátima Andrade e Pedro Jacob Christoffoleti
Importância
O gênero Amaranthus é composto por 60 espécies, das quais aproximadamente 20 possuem importância como plantas daninhas nos cultivos agrícolas em regiões tropicais e subtropicais (KISSMANN; GROTH, 1997). No Brasil, cerca de 10 espécies têm ocorrência, sendo as mais encontradas: A. hybridus (caruru-roxo), A. deflexus (caruru-rasteiro), A. lividus (caruru-folha-de-cuia), A. retroflexus (caruru-gigante), A. spinosus (caruru-de-espinho) e A. viridis (caruru-demancha) (CARVALHO et al., 2006).
Quando infestam culturas agrícolas, os carurus podem ser caracterizados como plantas de difícil manejo, devido ao extenso período de germinação do banco de sementes, rápido crescimento e desenvolvimento, elevada produção de sementes viáveis, longa viabilidade de suas sementes no solo e dificuldade na identificação das diferentes espécies no campo (HORAK; LOUGHIN, 2000; CARVALHO, 2015). O hábito de crescimento agressivo e a enorme produção de sementes oferecem às plantas do gênero Amaranthus grande competitividade com as culturas por luz, água e nutrientes (GUO; AL-KHATIB, 2003; SILVA et al., 2010; BARROSO et al., 2012).
Além das características citadas, a ocorrência de biótipos resistentes no campo atribui grande importância ao gênero Amaranthus, com destaque para A. palmeri e A. hybridus. No Brasil, no ano de 2015, foi relatado a ocorrência de Amaranthus palmeri resistente ao glifosato em áreas agrícolas do estado de Mato Grosso (CARVALHO et al., 2015). No mesmo ano também se confirmou a resistência múltipla ao herbicida glifosato e aos herbicidas inibidores da ALS (GONÇALVES NETTO et al., 2016). Recentemente, um novo caso de A. hybridus com resistência múltipla ao glifosato e inibidores da ALS foi constatado no Paraná (PENCKOWSKI; MASCHIETTO, 2019). Os casos de resistência do gênero Amaranthus são preocupantes, pois pode estar ocorrendo a hibridação interespecífica e a transferência do gene de resistência à herbicidas a outras espécies de caruru (GAINES et al., 2012).
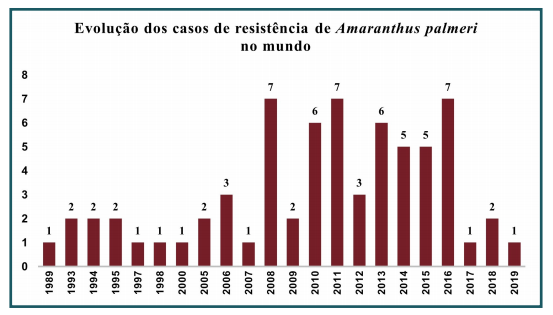
No caso do Amaranthus palmeri existem hoje no total de 68 casos de resistência reportados no mundo, sendo dois destes no Brasil (Tapurah – MT e Ipiranga do Norte – PR). Esses casos estão também distribuídos nos países: Argentina, Israel, México, Espanha e Estados Unidos. Aproximadamente 91% desses casos ocorrem nos Estados Unidos.
Nesse sentido, já foram relatados resistência a oito mecanismos de ação, sendo que 39% dos casos referem-se à resistência a EPSPS, 15% a herbicidas inibidores da ALS e 16% a resistência múltipla aos herbicidas inibidores da EPSPS e ALS.
O primeiro caso de A.palmeri resistente no mundo ocorreu em 1989, nos Estados Unidos, ao herbicida trifluralina. A partir dessa data, passaram-se 30 anos e foram relatados no total 68 casos, o que na média resulta em 2,3 casos de resistência novos por ano.
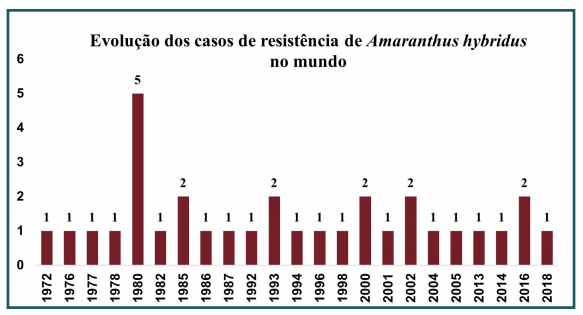
Para o Amaranthus hybridus há no total 32 casos relatados no mundo, com um caso relatado no Brasil. Desses casos, já foram relatados resistência nos países: Argentina, Bolívia, Canadá, França, Israel, Itália, África, Suíça e Estados Unidos. A maioria dos casos, está concentrado na Estados Unidos (53%) e Argentina (16%).
O primeiro relato de resistência foi registrado em 1972, nos Estados Unidos, com o herbicida atrazina. Desde então, são 46 anos que produtores e pesquisadores lidam com essa problemática, o que na média resulta em 1,4 caso novo a cada ano.
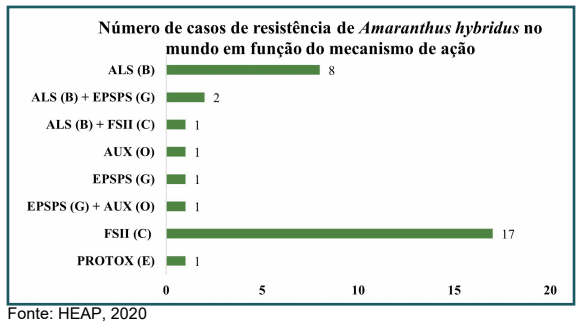
Até o momento, foram registrados resistência a 5 mecanismos de ação, sendo a maioria dos casos referentes aos herbicidas inibidores do fotossistema II (53%) e ALS (25%), respectivamente.
Identificações dos espécies
A identificação correta de espécies no campo é determinante no manejo de plantas daninhas, pois define a escolha dos herbicidas que podem ser utilizados para o controle. No campo, a identificação de espécies de Amaranthus não é simples, pois as espécies possuem elevada plasticidade fenotípica (CARVALHO, S. J. P.; CHRISTOFFOLETI, P. J; 2007), além da possibilidade de hibridação (GAINES et al., 2012).
- Amaranthus palmeri
O A. palmeri é uma espécie dióica, ou seja, parte das plantas de uma população tem somente flores femininas e outra parte, somente flores masculinas. Essa é uma característica que facilita a identificação de A. palmeri, uma vez que a maioria das outras espécies de caruru já identificadas no Brasil têm flores masculinas e femininas na mesma planta, sendo classificadas como monoicas. As sementes são produzidas somente nas plantas com flores femininas, mas há um detalhe importante e agravante da reprodução da espécie: flores femininas podem produzir sementes mesmo sem a ocorrência de polinização (LEGLEITER; JOHNSON, 2013). Além disso, na inflorescência das plantas femininas há a presença de folhas rudimentares (brácteas) duras que podem ser facilmente percebidas ao serem tocadas (Figura 1).
As formas das folhas podem variar bastante dentro uma única espécie, no entanto, as folhas de A. palmeri são mais largas e ovais e apresentam pecíolo longo que pode ser maior que o limbo foliar. Na ponta da folha, nota-se uma pequena reentrância (invaginação) onde se localiza um pequeno espinho. Entretanto, a presença deste espinho pode ocorrer também em outras espécies como o A. hybridus. Na axila das folhas e na inserção dos ramos nos caules também são encontradas estruturas espinescentes. Além disso, outra característica que aparece eventualmente, é a presença de uma marca d ́ água branca ou uma mancha esbranquiçada nas folhas na forma de “V” (LEGLEITER; JOHNSON, 2013) (Figura 1).
- Amaranthus hybridus
A principal característica que diferencia as duas espécies em questão de Amaranthus é a estrutura das flores, sendo o A. hybridus caracterizado como uma espécie monoica, ou seja, as flores femininas e masculinas estão presentes na mesma planta. Como características similares podemos citar o pecíolo longo, o espinho na extremidade da folha e a marca d ́água em forma de “V” nas folhas (Figura 1).
Além disso, trata-se de uma planta anual, ereta e com folhas lanceoladas dispostas de forma alterna helicoidal. Possui inflorescência terminal e axilar, sendo que a inflorescência axilar aparece apenas nas axilas das folhas superiores. Essa planta possui duas subespécies sendo elas: Amaranthus hybridus var. paniculatus e Amaranthus hybridus var. patulus. As duas subespécies se diferenciam devido a coloração da inflorescência, sendo o A. hybridus var. paniculatus caracterizado pela presença de inflorescência paniculada terminal de coloração roxa e o A. hybridus var. patulus com inflorescência paniculada terminal de cor esverdeada (Figura 1).
As flores femininas possuem tépalas lanceoladas e as flores masculinas possuem cinco estames. A flor masculina e a flor feminina ficam protegidas por 2 brácteas do tamanho ou pouco maiores que as tépalas e ligeiramente aristadas. Os frutos são deiscentes do tipo pixídio (LORENZI, 2000; SENNA et al., 2015) (Figura 1).
Controle
No Brasil, há vários relatos sobre a dificuldade em manejar áreas infestadas por diferentes espécies do gênero Amaranthus. Nesse sentido, cabe ressaltar a importância do manejo integrado de plantas daninhas (MIPD) que consiste na associação de técnicas químicas e não químicas para a prevenção e controle de plantas daninhas resistentes a herbicidas. Por meio das estratégias não químicas (rotação de culturas, medidas culturais e mecânicas) há a mortalidade de ambos os biótipos de plantas daninhas (suscetível e resistente) e a pressão de seleção é mantida. Já as estratégias químicas (herbicidas) podem ser usadas para reduzir a pressão de seleção por meio do uso de diferentes mecanismos de ação a fim de manter a diversidade de biótipos no banco de sementes do solo.
Estratégias de Manejo
1 – Rotação das Culturas
A rotação de culturas proporciona maior oportunidade de usar herbicidas com diferentes mecanismos de ação na área. Além disso, considerando a facilidade de dispersão e a alta produção de sementes de Amaranthus spp. a rotação de culturas é uma estratégia importante para modificar também as condições em que a espécie irá crescer e se desenvolver, pois a variação do espaçamento entrelinhas ou da densidade de plantas na linha pode contribuir para a redução da interferência da planta daninha sobre a cultura. Assim, como há diversificação de herbicidas usados em cada cultura, diminui-se a pressão de seleção de determinado mecanismo de ação no controle desta espécie. Por meio dessa prática previne-se o aparecimento dos biótipos resistentes, assim como facilita o manejo dos biótipos já existentes na área.
2 – Arranjo Manual
A alta prolificidade de ambas as espécies faz com que rapidamente o banco de sementes no solo seja ampliado ou reposto. Por isso, em condições de alta infestação, é importante a retirada das plantas que sobreviveram ao controle químico da área antes da emissão das inflorescências e da produção de sementes, pois estas podem facilmente rebrotar de caules remanescentes da capina, assim como se restabelecer pelo contato do solo com a raiz arrancada ou mesmo pela emissão de raízes em partes da planta em contato com o solo (IKEDA et al., 2019). É importante lembrar que as plantas arrancadas devem ser queimadas ou enterradas em altas profundidades.
3 – Colheita e limpeza de maquinários (https://youtu.be/bpIeHIq6NQE)
As sementes de caruru podem ser facilmente dispersas por maquinários, principalmente por colhedoras. Para evitar a dispersão dessa espécie para outros talhões ou propriedades vizinhas é recomendado que o produtor programe a colheita das áreas de alta infestação por último para não espalhar sementes para outras áreas. Além disso, ressalta-se a importância da limpeza de maquinários para evitar a introdução de biótipos na área e reduzir o acréscimo de sementes ao banco. É importante lembrar que a suspeita da introdução de A. palmeri no Brasil é oriunda de colhedoras de algodão sujas com sementes da planta daninha em questão.
De acordo com Schwartz-Lazaro et al. (2017) A. palmeri retém 98% das sementes até a maturidade da soja, o que faz com que essas sementes possam ser colhidas juntamente com os grãos e redistribuídas em outras áreas durante essa operação.
Outra via de introdução e disseminação de plantas daninhas é por meio das sementes da própria cultura. Por isso, é sempre recomendado utilizar sementes certificadas para que a produção agrícola não seja prejudicada ou inviabilizada.
4 – Cobertura do Solo
O uso de plantas de cobertura auxilia na supressão de plantas daninhas devido ao impedi-
mento físico, a redução das oscilações de temperatura e da qualidade da luz incidente no solo (JHA et al., 2010). Essa estratégia é uma boa opção principalmente pensando na entressafra. Nesse período há a multiplicação de muitas espécies enriquecendo o banco de sementes e a pressão de infestação. Logo, é recomendado não deixar as áreas em pousio na entressafra.
A planta de cobertura centeio é uma das mais estudadas na supressão de A. palmeri (LEGLEITER; JOHNSON, 2020). DeVore et al. (2011) descreveram redução de 85% na emergência de A. palmeri após revolvimento do solo no outono seguido da cobertura com o cereal centeio.
5 – Revolvimento do Solo
Assim como para as outras espécies de plantas daninhas, o controle do banco de sementes é essencial no manejo integrado. Segundo Ward (2013), a germinação e estabelecimento de plântulas de A. palmeri é amplamente reduzida quando as sementes são enterradas a profundidades a partir de 5 cm. O revolvimento do solo irá enterrar as sementes de Amaranthus abaixo da profundidade de emergência preferencial da espécie. Essa estratégia não proporciona controle total, mas pode reduzir o número de sementes que irá germinar. Segundo Legleiter; Johnson, (2020), em um campo totalmente infestado essa prática pode reduzir a população de A. palmeri em até 50%. Entretanto, os produtores devem observar o custo-benefício dessa prática levando em consideração o manejo de plantas daninhas e o sistema consolidado de plantio direto.
6 – Controle Químico
Ao se optar pela adoção do controle químico, é importante conhecer alguns fatores referentes aos herbicidas como seletividade à cultura, espectro de controle e efeito residual. A aplicação de herbicidas pós-emergentes tem como vantagem a facilidade da identificação das espécies do gênero Amaranthus, pois as plantas já estão emergidas. Entretanto, nessa condição há a maior influência do tamanho das plantas no momento da aplicação. É importante ressaltar que o controle químico de Amaranthus spp. nos estádios iniciais das plantas é essencial para a eficácia de controle, sendo o recomendado de 2-4 folhas com no máximo 5 cm de altura (GONÇALVES NETTO et al., 2019). A eficácia dos herbicidas é reduzida com o desenvolvimento das plantas. De acordo com Jordan; York (2010) as aplicações realizadas em plantas maiores que 8 cm resultam em nível de controle insatisfatório.
O uso de herbicidas residuais é interessante devido ao controle dessas espécies em estádios iniciais de desenvolvimento favorecendo a dianteira competitiva da lavoura e reduzindo as aplicações em pós-emergência. Isso pode ser explicado devido a atividade residual desses herbicidas que controla os primeiros fluxos germinativos e previnem a matocompetição inicial.
Outra prática envolvendo os herbicidas pré-emergentes é a aplicação de dois ou mais herbicidas para que haja a sobreposição do residual. Essa estratégia se baseia em aplicar um herbicida residual e antes que esse residual termine e novas plantas resistentes de A. palmeri e/ou A.hybridus germinem, é realizada a aplicação de um segundo herbicida para sobrepor o residual do primeiro. Essa sobreposição, também chamada de “overlapping” permite que o solo fique “limpo” por mais tempo e tem sido realizada com sucesso na Argentina e nos Estados Unidos (CHAHAL et al., 2018).
Mesmo considerando a eficácia dos herbicidas pré-emergentes para as espécies de caruru em questão é comum a ocorrência de novas emergências ao longo do ciclo da cultura em função do banco de sementes no solo e dos diversos fluxos de germinação.
7 – Estratégias de controle químico na soja, no milho e no algodão
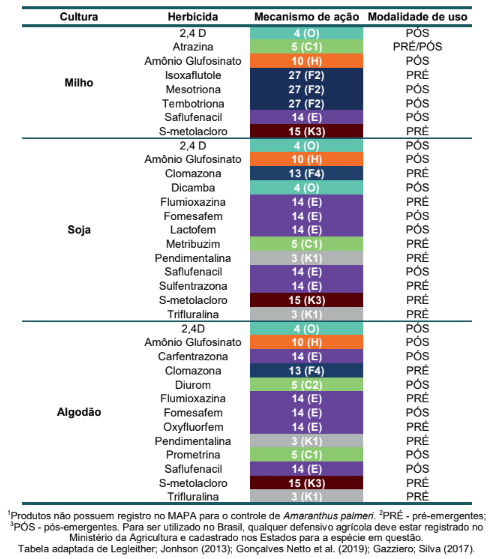
Diversos herbicidas disponíveis nas culturas da soja, milho e algodão podem controlar A.palmeri e A.hybridus de forma a proporcionar alternativas de controle com diferentes mecanismos de ação. Ressalta-se que nessa sessão realizou-se um compilado de herbicidas que podem ser usados para o controle dessas espécies, principalmente herbicidas que estão sendo eficazes na Argentina e Estados Unidos. Assim, para o uso de determinado herbicida, este deve possuir a indicação do uso na bula do produto e possuir registro no Ministério da Agricultura, Pecuária e Abastecimento (MAPA) (Tabela 1).
Observa-se a possibilidade de rotação de mecanismos de ação na cultura do milho em áreas infestadas com caruru resistente a ALS e EPSPS. Muitos produtores têm utilizado pré-
emergentes pertencentes a ácidos graxos de cadeia longa complementando na pós com inibidores do FSII associado ao HPPD. O uso de amônio glufosinato em cultivares de milho tolerantes a essa molécula também é uma alternativa viável para o controle na pós-emergência dessas plantas daninhas.
Em contraste com a cultura do milho, na soja a disponibilidade de herbicidas para a substituição do glifosato para o controle de A.hybridus e A.palmeri resistentes é limitado, principalmente na pós-emergência (Tabela 1). O controle na pós-emergência restringe-se basicamente aos herbicidas inibidores da protox, os quais por serem herbicidas de contato podem causar fitotoxicidade para a cultura da soja. Também na pós-emergência tem-se a opção do amônio glufosinato em cultivares tolerantes a esse herbicida. Além disso, para a utilização do 2,4 D ou dicamba na dessecação pré-plantio é importante salientar que o intervalo de plantio da soja pode variar entre 7 a 28 dias dependendo da dose, produto e condições ambientais (LEGLEITHER; JONHSON, 2013). Com o advento das tecnologias para a soja Enlist® (2,4 D, glifosato e amônio glufosinato) e Intacta 2Xtend® (dicamba e glifosato) abre-se também as possibilidades para o uso dos herbicidas auxínicos dentro da cultura.
O uso dos herbicidas pré-emergentes na cultura do algodão é uma ferramenta importante devido a restrição de possibilidades para o controle na pós-emergência. Além disso, devido ao lento estabelecimento da cultura essa modalidade de herbicidas ganha mais notoriedade.
Para a cultura do algodão, antes da semeadura, o herbicida 2,4 D tem sido usado na dessecação. Essa recomendação deve ser realizada com cautela respeitando o intervalo mínimo entre o uso do herbicida e a semeadura do algodão. Dependendo da cobertura vegetal e época de semeadura pode-se fazer a aplicação sequencial de herbicidas com a associação de herbicidas residuais em pré-emergência na segunda aplicação.
Para o controle em pré-emergência os ingredientes ativos mais utilizados visando o controle de caruru no algodão são a trifluralina e o S-metalacloro, geralmente em associação ao diuron (CAVENAGHI; GUIMARÃES, 2015). Cabe ressaltar ainda a possibilidade do uso de herbicidas inibidores da protox para a rotação de herbicidas na cultura.
Considerando o A. hybridus e A. palmeri resistentes a EPSPS e herbicidas inibidores da ALS o uso de variedades transgênicas a exemplo do amônio glufosinato, também é uma boa opção para alternar os mecanismos de ação visando o controle dessas espécies. Na pós-emergência, o controle fica restrito aos herbicidas inibidores da PROTOX e FSII que podem ser aplicados em jato dirigido.
Tabela 1. Herbicidas registrados para a cultura do milho, soja e algodão no Brasil para o controle de A. hybridus e que demonstram ser efetivos nos Estados Unidos e Argentina para o controle de biótipos de A. palmeri resistente a inibidores da ALS + EPSPS.
8 – Monitoramento
O monitoramento de plantas daninhas resistentes nos talhões deve ser realizado frequentemente observando-se principalmente a presença de escapes e reboleiras. Destaca-se também a ocorrência dessas plantas daninhas em áreas não agricultáveis como beiradas de estradas, canais de irrigação, cercas que podem servir de foco de contaminação para outras áreas.
O monitoramento é de extrema importância para produtores e para a indústria de insumos,
pois possibilita a detecção precoce dos casos de resistência e permite que estratégias para o manejo dessas plantas daninhas sejam implementados visando a sustentabilidade da produção agrícola.
Referências
ANDRADE JUNIOR, E. R. et al. Alternativas para controle químico e identificação molecular de Amaranthus palmeri. Cuiabá: Instituto Mato-Grossense do Algodão, 2018. (IMAMT. Circular Técnica, 33).
BARROSO, A.A.M. et al. Efeito da densidade e da distância de caruru-de-mancha e amendoim-bravo na cultura do feijoeiro. Planta Daninha, Viçosa – MG, v.30, n.1, p.47-53, 2012.
CARVALHO, S. J. P.; CHRISTOFFOLETI, P. J. Estimativa da área foliar de cinco espécies do gênero Amaranthus usando dimensões lineares do limbo foliar. Planta Daninha, v. 25, n. 2, p. 317-324, 2007.
CARVALHO, S. J. P.; et al. Detection of glyphosate-resistant Palmer Amaranth (Amaranthus palmeri) in agricultural areas of Mato Grosso, Brazil. Planta Daninha, Viçosa – MG, v. 33, n. 3, p. 579-586, 2015.
CARVALHO, S.J.P. Características biológicas e suscetibilidade a herbicidas de cinco espécies de plantas daninhas do gênero Amaranthus. 2006. 96 p. Dissertação (Mestrado em Agronomia – Área de Fitotecnia) – Escola Superior de Agricultura “Luiz de Queiroz”, Universidade de São Paulo, Piracicaba, 2006.
CAVENAGHI, A. L.; GUIMARÃES, S. C. Manejo de plantas daninhas do gênero Amaranthus na cultura do algodão. In: INOUE, M. H. et al. Manejo de Amaranthus. RiMa Editora, São Carlos, 2015.
CHAHAL, P. S. et al. Overlapping residual herbicides for control of photosystem (PS) II-and 4-hydroxyphenylpyruvate dioxygenase (HPPD)-inhibitor-resistant Palmer amaranth (Amaranthus palmeri S. Watson) in glyphosate-resistant maize. Frontiers in Plant science, v. 8, p. 2231, 2018.
DEVORE, J. D. et al. Influence of deep tillage and a rye cover crop on Palmer amaranth emergence in cotton. Summaries of Arkansas Cotton Research, p. 119, 2011.
GAINES, T. A. et al. Interspecific hybridization transfers a previously unknown glyphosate resistance mechanism in Amaranthus species. Evolutionary Applications, v. 5, n. 1, p. 29–38, 2012.
GAZZIERO, D. L. P.; SILVA, A. F. Caracterização e manejo de Amaranthus palmeri. Documentos-Embrapa Soja, n. 384, 2017.
GONÇALVES NETTO, A. et al. Control of ALS-and EPSPS-Resistant Amaranthus palmeri by Alternative Herbicides Applied in PRE-and POST-Emergence. Planta Daninha, v. 37, 2019.
GONÇALVES NETTO, A. et al. Multiple resistance of Amaranthus palmeri to ALS and EPSPS inhibiting herbicide in the state of Mato Grosso, Brazil. Planta Daninha, Viçosa – MG, v.34, n.3, p.581-587, 2016.
GUO, P.; AL-KHATIB, K. Temperature effects on germination and growth of redroot pigweed (Amaranthus retroflexus), Palmer amaranth (A. palmeri), and common waterhemp (A. rudis). Weed Science, Lawrence, v. 51, n. 6, p. 869-875, 2003.
HEAP, I. International survey of resistant weeds. Disponível em:<http://weedscience.org/Home.aspx> Acesso em 10 novembro 2020.
HORAK, M.J.; LOUGHIN, T.M. Growth analysis of four Amaranthus species. Weed Science Lawrence, v.48, n.3, p.347-355, 2000.
IKEDA, F. S. et al. Estratégias de controle de Amaranthus palmeri resistente a herbicidas inibidores de EPSPs e ALS. Embrapa Agrossilvipastoril-Documentos (INFOTECA-E), 2019.
JHA, P. et al. Annual changes in temperature and light requirements for germination of palmer amaranth (Amaranthus palmeri) seeds retrieved from the soil. Weed Science, v. 58, p. 426-432, 2010.
JORDAN, D.; YORK, A. Optimizing palmer amaranth control with postemergence herbicides control. Raleigh: North Carolina State University, 2010. 2 p. (Cooperative Extension, AG 728-W).
KISSMANN, K. G.; GROTH, D. Plantas infestantes e nocivas. 2. ed. São Paulo, 1997.
LEGLEITER, T.; JOHNSON, B. Palmer Amaranth biology, identification, and management. Purdue Extension, WS-51, 2013. Disponível em: <https://www.extension.purdue.edu/extmedia/WS/WS-51-W. pdf> Acesso: 10 out. 2020.
LORENZI, H. Plantas daninhas do Brasil: terrestres, aquáticas, parasitas e tóxicas, Nova Odessa: Instituto Plantarum, 2000. 608p.
PENCKOWSKI, L. H.; MASCHIETTO, E. Suspeita de Amaranthus hybridus resistente ao herbicida glyphosate. Revista FABC, p. 20–21, 2019.
RAIMONDI, M. A. et al. Atividade residual de herbicidas aplicados ao solo em relação ao controle de quatro espécies de Amaranthus. Planta Daninha, v. 28, n. SPE, p. 1073-1085, 2010.
SENNA, L.R. Identificação de espécies de plantas daninhas do gênero Amaranthus L. (Amaranthaceae Juss.) no Brasil. In.: INOUE, M.H.; OLIVEIRJA JÚNIOR, R.S.; MENDES, K.F.; CONSTANTIN, J. Manejo de Amaranthus. São Carlos: RiMa Editora, 2015. p.1-20.
SILVA, B.P. et al. Interferência de caruru-de-mancha, maria-pretinha, picão-preto e tiririca em tomateiro industrial. Bragantia, Campinas, v.69, n.2, p.313-318, 2010.
WARD, S. M. et al. Palmer amaranth (Amaranthus palmeri): a review. Weed Technology, v. 27, n. 1, p. 12-27, 2013.
ZANATTA, J. F. et al. Teores de água no solo e eficácia do herbicida fomesafen no controle de Amaranthus hybridus. Planta Daninha, v. 26, n. 1, p. 143-155, 2008.
Fonte: Comitê de Ação a Resistência aos Herbicidas – HRAC-BR