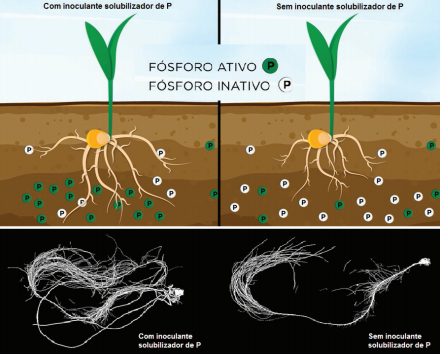
Introdução
O milho (Zea mays L.) é um dos principais cereais cultivados no mundo, sendo os Estados Unidos, a China e o Brasil os três maiores produtores. O Brasil se destaca como o terceiro maior produtor, com produção de 100,04 milhões de toneladas, na safra 2018/2019 (Acompanhamento da Safra Brasileira [de] Grãos, 2019). Esse cereal tem grande importância econômica e social no cenário agropecuário do país, sendo a maior parte da produção (70% a 85%) destinada à fabricação de ração animal e cerca de 15% são utilizados como matéria-prima para alimentação humana. Destaca-se ainda o seu emprego na indústria de alta tecnologia para a produção filmes, embalagens biodegradáveis e biocombustíveis (Ranum et al., 2014).
A produção agropecuária nacional se concentra na região dos Cerrados, onde os solos são predominantemente ácidos, pobres em nutrientes, com ênfase no fósforo (P), e com baixa capacidade de retenção de água (Novais; Smyth, 1999). Para o manejo eficiente da fertilidade do solo e da nutrição das plantas, o conhecimento das relações envolvidas no sistema solo-planta é fundamental.
Os microrganismos desempenham papel primordial na ciclagem de fósforo no solo, sendo capazes de transformar o fósforo insolúvel em formas solúveis e acessíveis às plantas (Owen et al., 2015).
A adição de inoculantes contendo esses microrganismos pode acelerar a liberação na rizosfera do fósforo inorgânico ou orgânico não disponíveis e enriquecer o solo biologicamente (Owen et al., 2015). Esses microrganismos ainda apresentam outros mecanismos de promoção de crescimento, como a solubilização de K, produção de fitormônios, enzimas, sideróforos, bioproteção contra patógenos, e podem, por meio de mecanismos secundários, aumentar a absorção de outros nutrientes e água pelo estímulo ao sistema de raízes (Gupta et al., 2015; Ribeiro et al., 2018).
Pesquisas do grupo de Microbiologia do Solo da Embrapa Milho e Sorgo indicaram que a adubação do milho com fertilizante organomineral pulverizado com microrganismos solubilizadores de fósforo (MSP) no sulco de semeadura resultou em produtividades similares ao milho adubado com superfosfato triplo. Houve ainda aumento do teor de P na parte aérea das plantas de milho e do P disponível no solo quando se realizou a inoculação com MSP (Oliveira et al., 2017). Amanullah e Khan (2015) observaram que a adubação fosfatada, seja com fonte mineral ou organomineral, associada a bactérias solubilizadoras de fósforo, aumentou a disponibilidade de P no solo e a absorção pela planta, o que resultou em aumento da produtividade do milho. A aplicação do inoculante na semeadura foi mais favorável quando comparada à aplicação aos 15 e 30 dias depois da semeadura.
Entre os microrganismos promotores de crescimento de plantas, o gênero Bacillus tem se destacado, compreendendo um grupo de bactérias Gram-positivas amplamente distribuídas no ambiente, composto por, aproximadamente, 360 espécies que apresentam características fisiológicas, metabólicas e fenotípicas distintas (http://www.bacterio.net/bacillus.html). Diferentes espécies desse gênero têm sido relatadas como potenciais promotoras de crescimento de plantas em razão das características multifuncionais como a solubilização de fosfato (Wahyudi et al., 2011; Bahadir et al., 2018), a produção de ácido indol-acético (AIA) e outros fitormônios (Wahyudi et al., 2011; Mohite, 2013), a produção de sideróforos-quelantes específicos de íons ferro (Bjelić et al., 2018) e a capacidade de biocontrole de patógenos de plantas (Shafi et al., 2017).
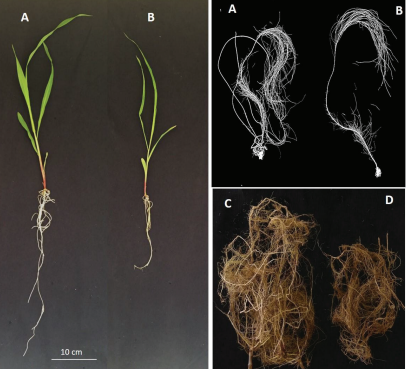
Além disso, inoculantes contendo cepas de Bacillus são considerados mais estáveis no ambiente por causa da capacidade de formação de endósporos, permitindo adaptação a condições abióticas extremas, como temperaturas, pH ou exposição a pesticidas (Bahadir et al., 2018). Entretanto, nem todas as cepas de Bacillus possuem as mesmas características. Com base em resultados de laboratório e de casa de vegetação, foram selecionadas as cepas B119 (Bacillus megaterium) e B2084 (Bacillus subtilis), eficientes na solubilização e mineralização de fósforo e promoção de crescimento de plantas (Figura 1) (Oliveira et al., 2009, 2013; Ribeiro et al., 2018) para a recomendação de produção de inoculantes industriais.
O objetivo desse trabalho foi avaliar o efeito da inoculação com as cepas Bacillus subtilis B2084 e B. megaterium B119, aplicadas isoladamente ou em mistura (BiomaPhos®), na produtividade de grãos de milho em condições de campo.
O BiomaPhos é um produto que contém a tecnologia Embrapa de aumentar a eficiência de uso do fósforo por microrganismos para as plantas, o que pode resultar em menores doses de fertilizante e, consequentemente, menos dispêndio de energia na produção e no transporte. Além disso, aumentando a produtividade das culturas, diminui a pressão sobre novas áreas e aumenta a sustentabilidade dos atuais sistemas de produção. Assim, representa uma contribuição para atingir a meta ODS 12, que visa garantir sistemas sustentáveis de produção de alimentos e implementar práticas agrícolas resilientes, que aumentem a produtividade e a produção, que ajudem a manter os ecossistemas, que fortaleçam a capacidade de adaptação às mudanças climáticas, às condições meteorológicas extremas, secas, inundações e outros desastres, e que melhorem progressivamente a qualidade da terra e do solo.
Materiais e Métodos
Efeito das cepas B119 (Bacillus megaterium) e B2084 (Bacillus subtilis) inoculadas isoladamente
Os experimentos de campo foram conduzidos em área da Embrapa Milho e Sorgo, localizada em Sete Lagoas-MG, Brasil (19º 28’S, 44º 15’W; 761 m de altitude) e na Embrapa Arroz e Feijão, em Santo Antônio de Goiás-GO, Brasil (16° 28´S, 49°17´W; 766 m de altitude), em três safras, nos anos agrícolas de 2014/2015, 2015/2016 e 2016/2017.
Em Sete Lagoas, os experimentos foram conduzidos em solo classificado como Latossolo Vermelho distrófico típico, fase cerrado, com baixo teor de fósforo. O clima em Sete Lagoas é o Cwa, segundo Köppen e Geiger, tropical de altitude, com índice pluviométrico anual de 1.382,7 mm (Guimarães et al., 2010) e temperatura média anual de 21,6 °C. Em Santo Antônio de Goiás-GO, o solo é classificado como Latossolo Vermelho-Escuro, textura argilosa, fase cerradão subperenifólio e de fertilidade construída. O clima local é Aw, tipo tropical de savana, megatérmico. A temperatura média anual é de 23,1 °C, e a precipitação pluvial média anual é de 1.472,8 mm. A adubação foi realizada com base nos resultados da análise química (Tabela 1) e recomendação para a cultura do milho.
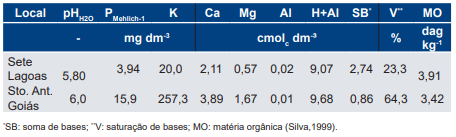
Tabela 1. Análise química de amostras de solos dos locais onde foram conduzidos os experimentos de campo em Sete Lagoas e Santo Antônio de Goiás.
Para cada cepa (Bacillus subtilis B2084 ou Bacillus megaterium B119) foram conduzidos três experimentos sob delineamento em blocos ao acaso, com 3 tratamentos: controle sem adubação com P (P0), superfosfato triplo (ST) e fosfato triplo mais o inoculante de cada cepa, em quatro repetições. O híbrido utilizado foi 30F53 (Pioneer Sementes).
Na adubação de semeadura foram aplicados 300 kg/ha do formulado 20-00-20 mais 100 kg/ha de P2O5 como superfosfato triplo (ST), exceto no controle sem P. Na adubação de cobertura foram empregados 140 kg/ha de N (ureia), aos 27 e aos 50 dias após a semeadura (70 kg/ha por aplicação). O milho foi cultivado com espaçamento de 0,7 m entre linhas e população de 75.000 plantas/ha. As parcelas foram compostas por quatro linhas de cinco metros, considerando-se um metro de bordadura de cada lado.
Para o preparo do inoculante, os microrganismos foram crescidos em caldo nutritivo TSB, por três dias, a 28± 2 °C, sob agitação constante de 120 rpm. Após esse período, as culturas foram centrifugadas por 10 minutos, a 6.000 rpm e ressuspendidas em solução salina [0,85% (m/v) NaCl]. As suspensões bacterianas foram ajustadas à absorbância igual a 1, em comprimento de onda de 540 nm, correspondente a uma densidade de aproximadamente 108 células/mL. Em seguida, elas foram adicionadas ao veículo (carvão ativado vegetal moído), na proporção de 30% (m/v) do total de inoculante líquido (100 mL/ha). O inoculante (bactéria + veículo) foi peletizado às sementes de milho com goma de fécula de mandioca a 4% (m/v) em água.
O controle de pragas e doenças, a adubação e os demais tratos culturais foram realizados conforme recomendação para a cultura (Cruz, 2010).
Ao final do ciclo da cultura, foi avaliada a produtividade de grãos de milho (kg/ha). Para a determinação de P nos grãos foi utilizada a metodologia de Nogueira e Souza (2005). Multiplicaram-se os dados de matéria seca dos grãos pelos teores de P, obtendo-se o acúmulo de P nos grãos.
Efeito das cepas B119 (Bacillus megaterium) e B2084 (Bacillus subtilis) inoculadas em mistura (BiomaPhos)
Para avaliar o efeito da aplicação conjunta das duas cepas no tratamento de sementes de milho do híbrido 30F53, foram realizados experimentos em Santa Maria-RS e Palotina-PR, em delineamento em blocos ao acaso, com 3 repetições, com os seguintes tratamentos: controle (sem adubação fosfatada), aplicação de 50% da dose recomendada de P, 100% da dose recomendada de P e 50% da dose recomendada de P mais inoculação conjunta com as cepas B119 e B2084. A recomendação de adubação foi realizada conforme análise química do solo. A produção do inoculante e demais avaliações e tratos culturais foram realizados conforme descrito anteriormente.
Os resultados dos ensaios com as cepas, isoladas ou em mistura, foram submetidos inicialmente ao teste de normalidade das variáveis e homogeneidade das variâncias. Em seguida, foi realizada análise de variância (ANOVA) e o teste de Scott-Knott foi aplicado para os casos em que houve significância estatística pelo teste F da ANOVA, considerando-se o nível de 5% (Ferreira, 2011).
Além dos experimentos, o efeito da inoculação conjunta das duas cepas foi avaliado em lavouras em áreas comerciais, com auxílio da Empresa Simbiose®, nos estados da Bahia, do Mato Grosso, Mato Grosso do Sul e de Goiás. Em todos os locais foram selecionadas áreas homogêneas de 20 ha, onde a metade (10 ha) recebeu sementes inoculadas e a outra metade recebeu sementes não inoculadas. O híbrido empregado foi 30F53 (Pioneer Sementes). O controle de pragas e doenças, a adubação e os demais tratos culturais foram realizados conforme recomendação para a cultura em cada região (Cruz, 2010). Ao final do ciclo da cultura, foi determinada a produtividade de grãos (kg/ha) colhendo-se separadamente 3 faixas com 3 ha nas áreas com e sem inoculante. As médias de produtividade provenientes de áreas inoculadas e não inoculadas, para cada estado, foram comparadas com auxílio do teste t (P ≤ 0,05).
Resultados
Efeito das cepas B119 (Bacillus megaterium) e B2084 (Bacillus subtilis) inoculadas isoladamente
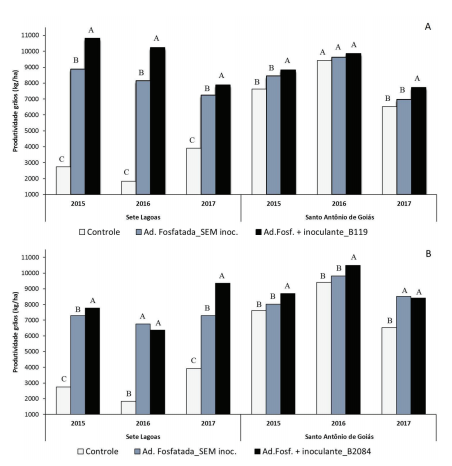
Em geral, houve efeito significativo dos tratamentos nas safras 2015, 2016 e 2017, em Sete Lagoas e Santo Antônio de Goiás (Figura 2). A inoculação da cepa B119 de B. megaterium resultou em aumentos significativos de produtividade, exceto em Santo Antônio de Goiás em 2016 (Figura 2A). Considerando os seis experimentos, a produtividade média aumentou em 16% em Sete Lagoas e 7% em Santo Antônio de Goiás com a combinação da inoculação da cepa B119 e adubação fosfatada em relação a apenas adubação fosfatada. Houve ainda, nas duas áreas, maior exportação de fósforo pelos grãos das plantas inoculadas com B. megaterium (cepa B119) em relação ao controle com fósforo e sem inoculação e em relação ao controle absoluto sem adubação e sem inoculação (Figura 3A).
A inoculação da cepa B2084 de B. subtilis aumentou significativamente a produtividade de grãos de milho em quatro de seis experimentos em relação ao tratamento com fósforo e sem inoculação (Figura 2B). Considerando os seis experimentos, a produtividade aumentou 11,4% em Sete Lagoas e 5% em Santo Antônio de Goiás com a inoculação de B2084. Houve aumento significativo na exportação de fósforo pelos grãos das plantas que receberam adubação fosfatada e foram inoculadas com a cepa B2084 em relação àquelas que receberam somente adubação fosfatada (Figura 3B).
Efeito das cepas B119 (Bacillus megaterium) e B2084 (Bacillus subtilis) inoculadas em mistura (BiomaPhos®)
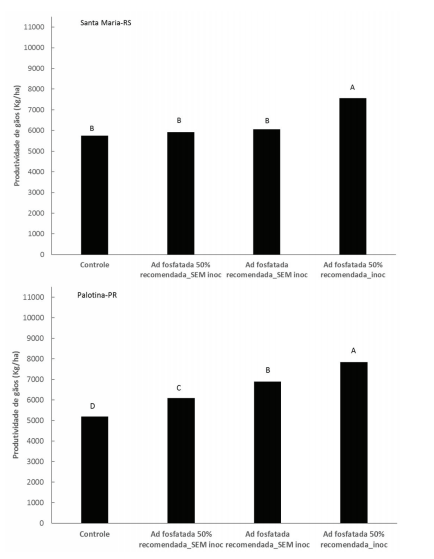
A mistura das duas cepas (inoculante BiomaPhos®) no tratamento de sementes resultou em ganhos significativos de produtividade nos dois locais avaliados (Figura 4). Tanto em Santa Maria quanto em Palotina a produtividade de grãos foi maior nas plantas que receberam 50% da adubação fosfata associada à inoculação com as duas estirpes. Em Santa Maria, a inoculação aumentou a produtividade em 27,7%, enquanto em Palotina o ganho foi de 28,7% para a mesma dose de P (Figura 4).
Nas avaliações realizadas em áreas de produtor, onde as adubações com fósforo foram aplicadas conforme recomendação local, houve aumento de produtividade por causa da inoculação: Bahia 7,8%, Mato Grosso do Sul 10,7%, Mato Grosso 17,6% e Goiás 8,3% (Figura 5). Considerando todos os locais, o ganho médio de produtividade com a inoculação foi de 8,9%.


produtividade de grãos de milho em lavouras comerciais cultivadas na Bahia, no Mato Grosso do Sul, Mato Grosso e em Goiás. Pares de médias, para cada estado, seguidos pela mesma letra, não diferem entre si pelo teste t (P ≤ 0,05).
Discussão
A inoculação com Bacillus subtilis (B2084), ou Bacillus megaterium (B119), resultou em ganhos médios de produtividade de 13,7% em Sete Lagoas e 6,5% em Santo Antônio de Goiás. Um inoculante à base de fungo solubilizador de fosfato, Penicillium bilaii, promoveu o aumento médio de produtividade do milho em solos mais férteis em 6% (Leggett et al., 2007). Breedt et al. (2017) encontraram aumentos de 24 a 34% na produtividade de milho ao inocularem microrganismos solubilizadores de fosfato, incluindo Bacillus. Em experimentos em campo, a inoculação de sementes de milho com Penicilium oxalicum, em associação com pó de rocha fosfática, proporcionou aumento significativo do crescimento, produtividade e teor de P das plantas (Singh; Reddy, 2011). Breedt et al. (2017), inoculando cepas de microrganismos solubilizadores de fosfato em milho, incluindo Bacillus, encontraram aumentos de 24% a 34% na produtividade de grãos.
Em relação ao controle sem adubação fosfatada e sem inoculação, os resultados de ganhos de produtividade considerando-se o efeito isolado das duas cepas, sem a adubação fosfatada, chegaram a 50%. Esses dados corroboram Patil et al. (2012), em que a inoculação com fungos solubilizadores de fosfato proporcionou ganhos de 20-23% de produtividade de milho em relação ao controle.
O efeito da inoculação em milho, em condições controladas e no campo, também foi evidenciado com estirpes bacterianas solubilizadoras de fosfato dos gêneros Serratia e Pseudomonas, que promoveram aumento do acúmulo de P, do crescimento de até 66% e de produtividade de até 85% em comparação com o controle não inoculado (Hameeda et al., 2008). Em condições controladas, a inoculação do milho com MSP e a adubação com fosfato de rocha proporcionaram aumento do comprimento das raízes em 11% e da massa seca em 35% (Manzoor et al., 2017), e em trabalhos da nossa equipe ocorreu aumento do conteúdo de P em plantas de milheto proporcional ao ganho de massa seca (Oliveira et al., 2013).
O uso combinado das cepas B119, isolada da rizosfera de milho, e B2084, endofítica, foi eficiente no aumento da produtividade do milho. A principal razão para o interesse na bactéria endofítica é a constatação de que, se esta puder ser reintroduzida na fase endofítica, pode estabelecer uma relação mais estável com a planta em comparação com os microrganismos rizosféricos (Szilagyi-Zecchin et al., 2014). Confirmando que microrganismos endofíticos são importantes para a solubilização de fosfato, Chen et al. (2014) observaram que Pantoea dispersa, isolada das raízes de mandioca, dissolveu efetivamente Ca3(PO4)2, FePO4 e AlPO4, pela produção de salicilato, ácido benzenoacético e outros ácidos orgânicos. Além disso, a inoculação de P. dispersa resultou em aumento da concentração de P solúvel e da diversidade microbiana do solo, o que sugere que um endófito poderia se adaptar ao ambiente do solo e promover a liberação de P.
Conclusão
As cepas de Bacillus subtilis CNPMS B2084 e Bacillus megaterium CNPMS B119 foram eficientes em aumentar a produtividade de grãos de milho em relação aos tratamentos sem inoculação e com adubação fosfatada. Em razão de propriedades distintas que levam ao maior acúmulo de fósforo nos grãos, maximização da adubação fosfatada e aumento da produtividade com a inoculação de B119, rizosférica, e B2084, endofítica, recomenda-se o uso combinado das duas cepas para a produção de inoculante para a cultura do milho. Os resultados realizados com a combinação das duas cepas no inoculante BiomaPhos®, no Paraná, Bahia, Rio Grande do Sul, em Mato Grosso do Sul, Mato Grosso e em Goiás apresentaram produtividade superior significativa em relação ao controle sem o inoculante. Considerando todos os locais, o ganho médio de produtividade com a inoculação foi de 8,9%.
Autores:
- Christiane Abreu de Oliveira Paiva – 1 Eng. Agrôn., DCs em Biologia Vegetal, Pesquisadora da Embrapa Milho e Sorgo;
- Ivanildo Evódio Marriel – Eng. Agrôn., DCs em Agronomia, Pesquisador da Embrapa Milho e Sorgo;
- Eliane Aparecida Gomes – Bióloga, DCs em Genética e Melhoramento, Pesquisadora da Embrapa Milho e Sorgo;
- Luciano Viana Cota – ; Eng. Agrôn., DCs em Fitopatologia, Pesquisador da Embrapa Milho e Sorgo;
- Flávia Cristina dos Santos – Eng. Agrôn., DCs em Solos e Nutrição de Plantas, Pesquisadora da Embrapa Milho e Sorgo;
- Sylvia Morais de Sousa Tinoco – Bióloga, DCs em Genética e Biologia Molecular, Pesquisadora da Embrapa Milho e Sorgo;
- Ubiraci Gomes de Paula Lana – Químico, DCs em Genética, Analista da Embrapa Milho e Sorgo;
- Maycon Campos Oliveira – Bioquímico, DCs em Ciências Biológicas, Analista da Embrapa Milho e Sorgo;
- Bianca Braz Mattos – Bióloga, Ms em Microbiologia, Analista da Embrapa Solos;
- Vera Maria Carvalho Alves – Eng. Agrôn., DCs em Solos e Nutrição de Plantas, Pesquisadora da Embrapa Milho e Sorgo;
- Vitoria Palhares Ribeiro – Bióloga, estudante Doutorado Universidade Federal São Joao Del Rey;
- Reinaldo Vasco Junior – Técnico agrícola,Técnico da Embrapa Milho e Sorgo.
Onde obter mais informações:
BiomaPhos – https://bit.Iy/34GaqLa – Embrapa e Bioma lançam primeiro inoculante nacional para fósforo – https://bit.Iy/2R0eB0o
Conexão Ciência – BiomaPhos: https://bit.Iy/2QQ2anG
Nova tecnologia ajuda agricultores na adubação das lavouras: https:// globoplay.globo.com/v/8421357/
Referências
ACOMPANHAMENTO DA SAFRA BRASILEIRA [DE] GRÃOS: safra 2019/20: segundo levantamento. Brasília, DF: Conab, v. 7, n. 2, nov. 2019. 105 p. Disponível em <https://www.conab.gov.br/info-agro/safras/graos>. Acesso em: 18 nov. 2019.
AMANULLAH; KHAN, A. Phosphorus and compost management influence maize (Zea mays) productivity under semiarid condition with and without phosphate solubilizing bacteria. Frontiers in Plant Science, v. 6, article 1083, 2015.
BAHADIR, P. S.; LIAQAT, F.; ELTEM, R. Plant growth promoting properties of phosphate solubilizing Bacillus species isolated from the Aegean Region of Turkey. Turkish Journal of Botany, v. 42, n. 2, p. 183-196, 2018.
BJELIĆ, D.; MARINKOVIĆ, J.; TINTOR, B.; MRKOVAČKI, N. Antifungal and plant growth promoting activities of indigenous rhizobacteria isolated from maize (Zea mays L.) rhizosphere. Communications in Soil Science and Plant Analysis, v. 49, n. 1, p. 88-98, 2018.
BREEDT, G.; LABUSCHAGNE, N.; COUTINHO, T. A. Seed treatment with selected plant growth-promoting rhizobacteria increases maize yield in the field. Annals of Applied Biology, v. 171, n. 2, p. 229-236, 2017.
CHEN, Y.; FAN, J. B.; DU, L.; XU, H.; ZHANG, Q. Y.; HE, Y. Q. The application of phosphate solubilizing endophyte Pantoea dispersa triggers the microbial community in red acidic soil. Applied Soil Ecology, v. 84, p. 235-244, 2014.
CRUZ, J. C. (Ed.) Cultivo do milho. 6. ed. Sete Lagoas: Embrapa Milho e Sorgo, 2010. (Embrapa Milho e Sorgo. Sistema de produção, 1).
FERREIRA, D. F. Sisvar: a computer statistical analysis system. Ciência e Agrotecnologia, v. 35, n. 6, p. 1039-1042, 2011.
GUIMARÃES, D. P.; REIS, R. J. dos; LANDAU, E. C. Índices pluviométricos em Minas Gerais. Sete Lagoas: Embrapa Milho e Sorgo, 2010. 88 p. (Embrapa Milho e Sorgo. Boletim de Pesquisa e Desenvolvimento, 30).
GUPTA, G.; PARIHAR, S. S.; AHIRWAR, N. K.; SNEHI, S. K.; SINGH, V. Plant growth promoting rhizobacteria (PGPR): current and future prospects for development of sustainable agriculture. Journal of Microbial and Biochemical Technology, v. 7, n. 2, p. 96-102, 2015.
HAMEEDA, B.; HARINI, G.; RUPELA, O. P.; WANI, S. P.; REDDY, G. Growth promotion of maize by phosphate solubilizing bacteria isolated from composts and macrofauna. Microbiological Research, v. 162, n. 2, p. 234-242, 2008.
LEGGETT, M.; CROSS, J.; HNATOWICH, G.; HOLLOWAY, G. Challenges in commercializing a phosphate-solubilizing microorganism: Penicillium bilaiae, a case history. In: VELÁZQUEZ, E.; RODRÍGUEZ-BARRUECO, C. Developments in plant and soil sciences. Dordrecht: Springer, 2007. p. 215-222.
MANZOOR, M.; KALEEM ABBASI, M.; SULTAN, T. Isolation of phosphate solubilizing bacteria from maize rhizosphere and their potential for rock phosphate solubilization-mineralization and plant growth promotion. Geomicrobiology Journal, v. 34, p. 81-95, 2017.
MOHITE, B. Isolation and characterization of indole acetic acid (IAA) producing bacteria from rhizospheric soil and its effect on plant growth. Journal of Soil Science and Plant Nutrition, v. 13, n. 3, p. 638-649, 2013.
NOGUEIRA, A. R. A.; SOUZA, G. B. (Ed.). Manual de laboratórios: solo, água, nutrição vegetal, nutrição animal e alimentos. São Carlos: Embrapa Pecuária Sudeste, 2005. 334 p.
NOVAIS, R. F.; SMYTH, T. J. Fósforo em solo e planta em condições tropicais. Viçosa, MG: Universidade Federal de Viçosa, 1999. 399 p.
OLIVEIRA, C. A.; ALVES, V. M. C.; MARRIEL, I. E.; GOMES, E. A.; SCOTTI, M. R.; CARNEIRO, N. P.; GUIMARÃES, C. T.; SCHAFFERT, R. E.; SÁ, N. M. H. Phosphate solubilizing microorganisms isolated from rhizosphere of maize cultivated in an oxisol of the Brazilian Cerrado Biome. Soil Biology and Biochemistry, v. 41, n. 9, p. 1782-1787, 2009.
OLIVEIRA, C. A.; MARRIEL, I. E.; GOMES, E. A.; MATTOS, B. B.; SANTOS, F. C.; OLIVEIRA M. C.; ALVES, V. M. C. Metodologia de aplicação de microrganismos solubilizadores de fósforo em sementes visando melhor aproveitamento deste nutriente pelas plantas. Sete Lagoas: Embrapa Milho e Sorgo, 2013. 25 p. (Embrapa Milho e Sorgo. Boletim de Pesquisa e Desenvolvimento, 88).
OLIVEIRA, C. A.; SANTOS, F. C. dos; MARRIEL, I. E.; ALMEIDA, C. N. S.; GOMES, E. A.; MATTOS, B. B.; PASSOS, A. M. A. dos; ALBUQUERQUE FILHO, M. R. de; TEIXEIRA, P. C. Adubação fosfatada organomineral com pulverização de inoculante contendo microrganismos solubilizadores. Sete Lagoas: Embrapa Milho e Sorgo, 2017. 11 p. (Embrapa Milho e Sorgo. Circular Técnica, 236).
OWEN, D.; WILLIAMS, A.; GRIFFITH, G.; WITHERS, P. Use of commercial bioinoculants to increase agricultural production through improved phosphrous acquisition. Applied Soil Ecology, v. 86, p. 41-54, 2015.
PATIL, P. M.; KULIGOD, V. B.; HEBSUR, N. S.; PATIL, C. R.; KULKARNI, G. N. Effect of phosphate solubilizing fungi and phosphorus levels on growth, yield and nutrient content in maize (Zea mays). Karnataka Journal Agriculture Science, v. 25, n. 1, p. 58-62, 2012.
RANUM, P.; PEÑA-ROSAS, J. P.; GARCIA-CASAL, M. N. Global maize production, utilization, and consumption. Annals of the New York Academy of Sciences, v. 1312, p. 105-112, 2014.
RIBEIRO, V. P.; MARRIEL, I. E.; SOUSA, S. M. de; LANA, U. G. de P.; MATTOS, B. B.; PAIVA, C. A. O.; GOMES, E. A. Endophytic Bacillus strains enhance pearl millet growth and nutrient uptake under low-P. Brazilian Journal of Microbiology, v. 49S, p. 40-46, 2018.
SHAFI, J.; TIAN, H.; JI, M. Bacillus species as versatile weapons for plant pathogens: a review. Biotechnology & Biotechnological Equipment, v. 31, n. 3, p. 446-459, 2017.
SILVA, F. C. da (Org.). Manual de análises químicas de solos, plantas e fertilizantes. Brasília, DF: Embrapa Comunicação para Transferência de Tecnologia; Rio de Janeiro: Embrapa Solos; Campinas: Embrapa Informática Agropecuária, 1999. 370 p.
SINGH, H.; REDDY M. S. Eff ect of inoculation with phosphate solubilizing fungus on growth and nutrient uptake of wheat and maize plants fertilized with rock phosphate in alkaline soils. European Journal of Soil Biology, v. 47, n. 1, p. 30-34, 2011.
SZILAGYI-ZECCHIN, V. J.; IKEDA, A. C.; HUNGRIA, M.; ADAMOSKI, D.; KAVA-CORDEIRO, V.; GLIENKE, C.; GALLI-TERASAWA, L. V. Identifi cation and characterization of endophytic bacteria from corn (Zea mays L.) roots with biotechnological potential in agriculture. AMB Express, v. 4, p. 4-9, 2014.
WAHYUDI, A. T.; ASTUTI, R. P.; WIDYAWATI, A.; MERYANDINI, A.; NAWANGSIH, A. A. Characterization of Bacillus sp. strains isolated from rhizosphere of soybean plants for their use as potential plant growth for promoting rhizobacteria. Journal of Microbiology Indonesia, v. 3, n. 2, p. 34-40, 2011.
Fonte: Embrapa